Un trasplante de médula ósea transmite el alzhéimer a ratones sanos
Un estudio cambia el paradigma del alzhéimer de ser una enfermedad que se produce exclusivamente en el cerebro a una enfermedad más sistémica
Cinco personas desarrollaron alzhéimer tras una terapia con hormonas de crecimiento de cadáveres

Esta funcionalidad es sólo para registrados
Iniciar sesiónLa enfermedad de Alzheimer familiar se puede transmitir mediante un trasplante de médula ósea, según muestra un estudio publicado en la revista 'Stem Cell Reports'.
Cuando se llevó a cabo un trasplante de células madre de médula ósea de ratones portadores de una versión ... hereditaria de la enfermedad de Alzheimer a ratones de laboratorio normales, los receptores desarrollaron alzhéimer, y a un ritmo acelerado.
El estudio destaca el papel del amiloide que se origina fuera del cerebro en el desarrollo de la enfermedad de Alzheimer, lo que cambia el paradigma del alzhéimer de ser una enfermedad que se produce exclusivamente en el cerebro a una enfermedad más sistémica.
La enfermedad que te hace ver demonios
Rafael IbarraEl síndrome de 'Alicia en el país de las maravillas' o prosopometamorfopsia afecta la forma, el tamaño, el color y la posición de las características faciales
Teniendo en cuenta sus hallazgos, los investigadores creen que los donantes de sangre, tejidos, órganos y células madre deben ser examinados para detectar la enfermedad de Alzheimer para prevenir la transmisión involuntaria durante las transfusiones de productos sanguíneos y las terapias celulares.
La información no es nueva, ya que desde hace tiempo se sugiere que la enfermedad de Alzheimer puede tener formas adquiridas médicamente (iatrogénicas). Así, recientemente se publicó en 'Nature Medicine' los casos de cinco personas que recibieron tratamiento con hormona del crecimiento humano derivada de pituitarias de cadáveres durante la infancia (un tratamiento actualmente prohibido) que desarrollaron trastornos tempranos y progresivos en la cognición que cumplían con los criterios diagnósticos de la enfermedad de Alzheimer. Sin embargo, no hay evidencia de que pueda transmitirse en otros contextos, como la atención rutinaria o la vida diaria.
Estos estudios y el ahora publicado en 'Stem Cell Reports' apoyan la idea de que el Alzheimer es una enfermedad sistémica en la que los amiloides que se expresan fuera del cerebro contribuyen a la patología del sistema nervioso central. Según explica el autor principal e inmunólogo Wilfred Jefferies, de la Universidad de Columbia Británica (Canadá), «a medida que exploramos este mecanismo, la enfermedad de Alzheimer puede ser la punta del iceberg y necesitamos tener controles y pruebas de detección mucho mejores de los donantes utilizados en trasplantes de sangre, órganos y tejidos, así como en las transferencias de células madre derivadas de humanos o productos sanguíneos».
Alzhéimer familiar
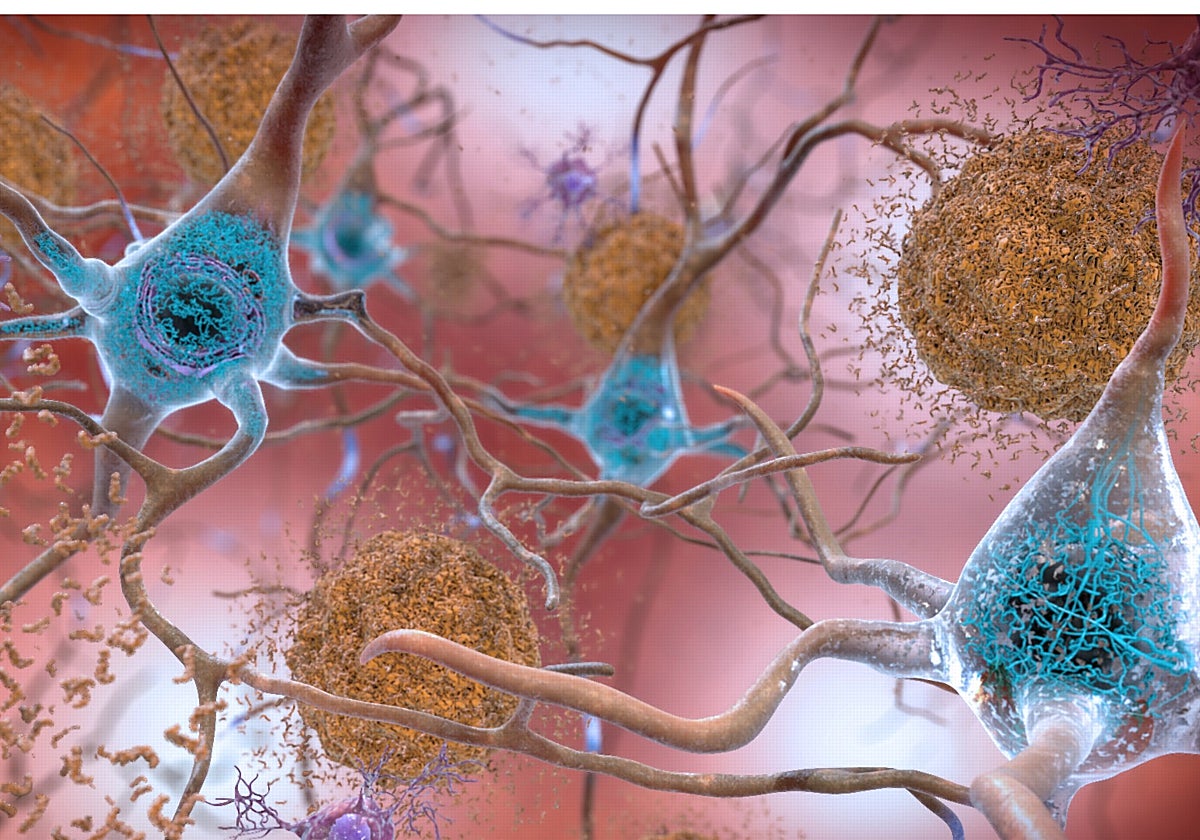
Para probar si una fuente periférica de amiloide podría contribuir al desarrollo del alzhéimer en el cerebro, los investigadores trasplantaron médula ósea que contenía células madre de ratones portadores de una versión familiar de la enfermedad: una variante del gen de la proteína precursora de amiloide humano (APP) que, cuando se escinde, se plega mal y se agrega, forma las placas amiloides que son un sello distintivo de la enfermedad de Alzheimer.
Los científicos realizaron trasplantes en dos cepas diferentes de ratones receptores: ratones desactivados para APP que carecían por completo de un gen APP y ratones que portaban un gen APP normal.
En este modelo de enfermedad de Alzheimer hereditaria, los ratones generalmente comienzan a desarrollar placas entre los 9 y 10 meses de edad, y los signos conductuales de deterioro cognitivo comienzan a aparecer entre los 11 y 12 meses de edad. Sorprendentemente, los receptores del trasplante comenzaron a mostrar síntomas de deterioro cognitivo mucho antes: a los 6 meses después del trasplante en los ratones knockout para APP y a los 9 meses en los ratones «normales».
En ratones, los signos de deterioro cognitivo se presentan como una ausencia de miedo normal y una pérdida de memoria a corto y largo plazo
«El hecho de que pudiéramos ver diferencias significativas de comportamiento y deterioro cognitivo en los knockouts de APP a los 6 meses fue sorprendente pero también intrigante porque simplemente mostró la aparición de la enfermedad que se estaba acelerando después de ser transferida», explica Chaahat Singh.
En ratones, los signos de deterioro cognitivo se presentan como una ausencia de miedo normal y una pérdida de memoria a corto y largo plazo. Ambos grupos de ratones receptores también mostraron claras características moleculares y celulares de la enfermedad de Alzheimer, incluidas barreras hematoencefálicas con fugas y acumulación de amiloide en el cerebro.
Al observar la transferencia de la enfermedad en ratones knockout para APP que carecían por completo de un gen APP, el equipo concluyó que el gen mutado en las células del donante puede causar la enfermedad y observar que los animales receptores que portaban un gen APP normal son susceptibles a la enfermedad sugiere que la enfermedad puede transmitirse a personas sanas.
Debido a que las células madre trasplantadas eran células hematopoyéticas, lo que significa que podían convertirse en células sanguíneas e inmunitarias, pero no en neuronas, la demostración de amiloide por parte de los investigadores en el cerebro de ratones knockout para APP muestra definitivamente que la enfermedad de Alzheimer puede resultar del amiloide que se produce fuera del sistema nervioso central.
Gen humano mutado
Por último, la fuente de la enfermedad en ratones es un gen APP humano que demuestra que el gen humano mutado puede transferir la enfermedad a una especie diferente.
En futuros estudios, los investigadores planean probar si el trasplante de tejidos de ratones normales a ratones con Alzheimer familiar podría mitigar la enfermedad y probar si la enfermedad también es transferible a través de otros tipos de trasplantes o transfusiones y ampliar la investigación sobre la transferencia de enfermedades. entre especies.
«En este estudio, examinamos el trasplante de médula ósea y células madre. Sin embargo será importante examinar si se produce una transmisión involuntaria de enfermedades durante la aplicación de otras formas de terapias celulares, así como examinar directamente la transferencia de enfermedades desde fuentes contaminadas, independientemente de los mecanismos celulares», advierte Jefferies.
Esta funcionalidad es sólo para suscriptores
Suscribete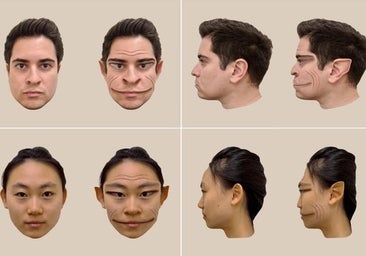
Esta funcionalidad es sólo para registrados
Iniciar sesiónEsta funcionalidad es sólo para suscriptores
Suscribete