CARDIOLOGÍA
El “reloj” inmune que controla las infecciones y la enfermedad cardiovascular
Investigadores del CNIC han demostrado la existencia de un “reloj” inmune que coordina los ciclos día/noche con la actividad de un tipo de leucocito denominado neutrófilo
S.Gutiérrez
Un “reloj” inmune coordina los ciclos día/noche con la actividad de un tipo de leucocito denominado neutrófilo. Lo ha visto un equipo del Centro Nacional de Investigaciones Cardiovasculares (CNIC) y que publica hoy sus resultados en la revista « Immunity », unos hallazgos que ... pueden tener múltiples implicaciones y de un alto valor clínico debido a la alta prevalencia de infecciones y enfermedades cardiovasculares en el mundo.
Noticias relacionadas
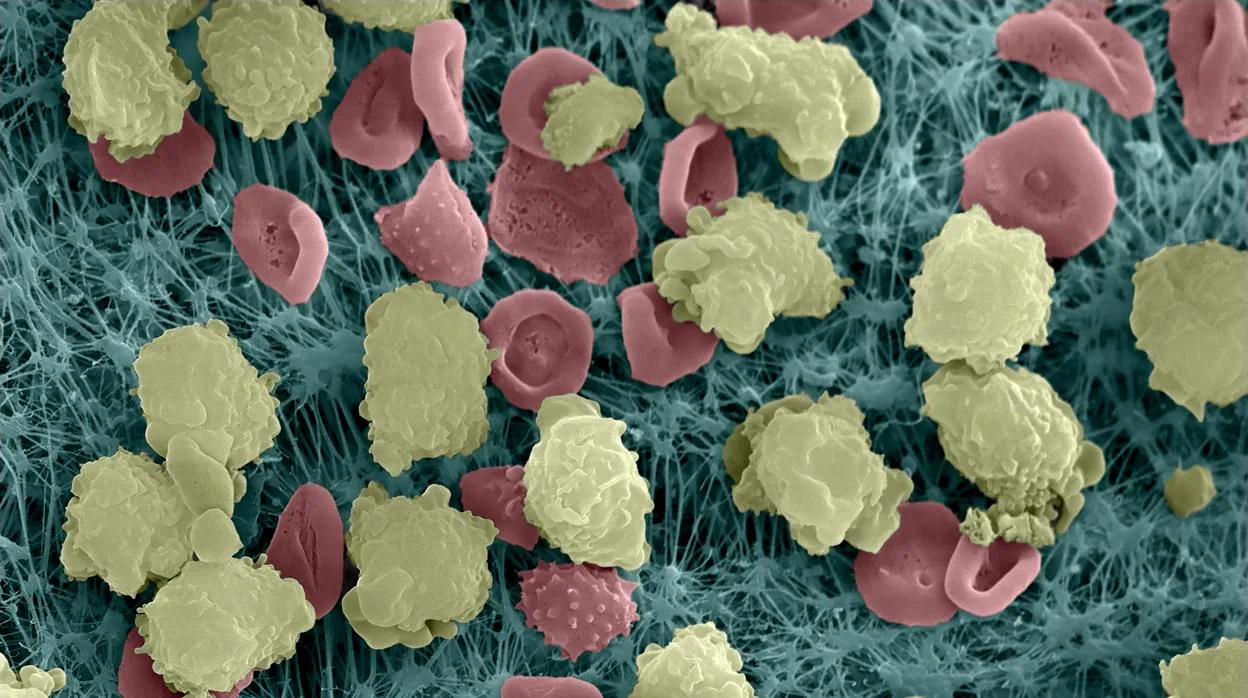
La principal línea de defensa del organismo son los neutrófilos, pero también son capaces de causar daño a las células sanas y al sistema cardiovascular. El reloj recién descubierto dicta cuándo éstas células deben ser activadas y cuándo eliminadas de la circulación sanguínea. Más exactamente, se ha identificado « una serie de moléculas en el núcleo y la membrana de los neutrófilos que responden a patrones diurnos de luz y oscuridad, y regulan su migración y ubicación dentro del organismo» , indica José María Adrover, primer autor del trabajo realizado por el grupo del CNIC de Andrés Hidalgo.
-kuh--220x220@abc.JPG)
Los investigadores recuerdan que e l mundo no está dominado por los humanos sino por miles de billones de seres microscópicos (bacterias, hongos y virus) que están en todas partes , que son esenciales para la vida en el planeta y con los que necesariamente debemos convivir. Dicha convivencia se ‘rompe’ cuando algunos de estos seres diminutos se introducen en nuestra sangre y órganos y se convierten en patógenos que causan enfermedad y muerte.
Los neutrófilos son la principal línea de defensa del organismo, pero también son capaces de causar daño a las células sanas y al sistema cardiovascular
El sistema inmune, y particularmente el neutrófilo, permite que esta convivencia sea pacífica al eliminar eficientemente los microorganismos que nos infectan. Sin embargo, esto genera un problema porque a menudo la respuesta inmune es desproporcionada y daña a los tejidos sanos . Esto, explica Andrés Hidalgo, «es lo que ocurre, por ejemplo, durante el infarto de miocardio, el ictus o el daño pulmonar agudo».
El dilema es, entonces, cómo controlar al sistema inmune para que proteja frente las infecciones, pero no cause daños colaterales al organismo.
Dilema biológico
Y esto es lo que ha hecho este grupo. Los autores han utilizado la tecnología más avanzada para seguir el comportamiento de estos leucocitos en distintos momentos del día. Además, en modelos animales de infarto, ictus e infecciones han demostrado que la manipulación de este reloj altera de manera dramática la respuesta inmune. «Los animales en los que manipulamos este reloj genéticamente se vuelven muy resistentes a infecciones, pero extremadamente sensibles a un infarto », señala Alejandra Aroca, una de las autoras del estudio. Finalmente, los autores también muestran que un reloj inmune similar puede existir en humanos.
Las implicaciones de este estudio pueden ser múltiples y de un alto valor clínico debido a la alta prevalencia de infecciones y enfermedades cardiovasculares en el mundo
Debido a que la mayoría de las muertes en países desarrollados ocurre por este tipo de daños cardiovasculares, la información que desvela este trabajo relevante. No hay que olvidar que la mayoría de los infartos ocurren a primera hora de la mañana ; es decir siguen un patrón circadiano. Puesto que los patrones circadianos en enfermedad cardiovascular, infecciones e inmunidad coincidían, el grupo estudió si había una relación causa-efecto entre ellos. «Observamos que, si eliminábamos el reloj en los neutrófilos de los ratones, entonces los patrones circadianos en la infección e infarto desaparecían -indica Adrover-; es decir, durante el día los neutrófilos causan más daño en caso de infarto, pero son más eficientes eliminando patógenos que invadan los tejidos. Si ahora somos capaces de controlar este reloj podemos aprovechar este fenómeno en favor de los pacientes».
Las implicaciones de este estudio pueden ser múltiples y de un alto valor clínico debido a la alta prevalencia de infecciones y enfermedades cardiovasculares en el mundo. «Por ejemplo -indica Hidalgo-, estamos buscando vías de manipular este reloj con fármacos para inducir un tipo de inmunidad diurna o nocturna, según interese en cada paciente».
Por lo tanto, concluyen, esta aproximación terapéutica, podría ser válida para aquellas personas con riesgo de eventos cardiovasculares y también pacientes inmunocomprometidos susceptibles a infecciones.
Esta funcionalidad es sólo para suscriptores
Suscribete
Esta funcionalidad es sólo para registrados
Iniciar sesiónEsta funcionalidad es sólo para suscriptores
Suscribete