CÁNCER DE TIROIDES
El uso de nanopartículas permite el tratamiento del cáncer tiroideo más agresivo
El carcinoma anaplásico de tiroides se asocia con una mortalidad cercana al 100% y una supervivencia de tan solo 3-5 meses
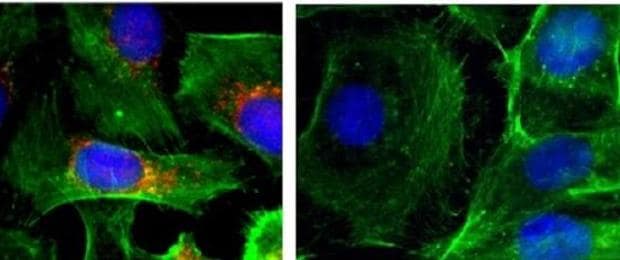
M. LÓPEZ
El carcinoma anaplásico de tiroides se corresponde con el tipo de cáncer más agresivo de la glándula tiroides. No en vano, la tasa de mortalidad asociada a este tipo de tumor es prácticamente de un 100%. Además, y dado que invade rápidamente todos los tejidos ... adyacentes y tiene una gran capacidad para migrar a otros órganos del cuerpo –la consabida ‘metástasis’–, la supervivencia asociada al tumor se establece en tan solo 3-5 meses. La buena noticia es que, según han mostrado distintos estudios, el uso del denominado ARN de interferencia –o ‘ARNi’, que permite la supresión de la expresión de genes específicos– podría ser eficaz, y mucho, en el tratamiento de este tumor. El problema es que aún no se ha encontrado la manera de transportar este ARNi a las células tumorales. O así ha sido hasta ahora, dado que investigadores del Hospital Brigham’s and Women de Boston (EE.UU.) parecen haber hallado la forma de lograrlo.
Concretamente, el estudio, publicado en la revista « Proceedings of the National Academy of Sciences », describe como el uso de nanopartículas permite el transporte de este ARNi a las células tumorales, lo que resulta en una supresión de la proliferación tumoral y en una reducción de las metástasis . Es más; además de con ARNi, las nanopartículas también están cargadas de un agente fluorescente, lo que posibilita comprobar que estas nanoplataformas –esto es, la suma de las nanopartículas, del ARNi y del agente fluorescente– alcanzan y se acumulan en las células del tumor.
Como explica Jinjun Shi, director de la investigación, «nuestras plataformas son ‘tratanósticas’ porque aúnan tanto el tratamiento como el diagnóstico del tumor en una única nanopartícula funcional. Esperamos que este estudio abra el camino al desarrollo de plataformas ‘tratanósticas’ para el transporte de ARNi guiado por imagen para el tratamiento de los tumores avanzados».
Nanoplataformas
Por lo general, los carcinomas anaplásicos de tiroides se producen, tal y como sucede en otros muchos tipos de cáncer, por una mutación en el gen ‘BRAF’. Por tanto, la solución consiste en utilizar un ARNi que se una específicamente a esta mutación y ‘silencie’ su expresión. De esta manera detendría el crecimiento del tumor y se evitaría su expansión a otros órganos, generalmente el pulmón.
Entonces, el tratamiento está claro: hay que hacer llegar el ARNi a las células tumorales. El problema es que la administración de moléculas de ARNi es completamente inútil, pues son degradadas por las enzimas del organismo o filtradas a través de los riñones. Y aún en el caso, altamente improbable, de que alcanzaran el tumor, serían incapaces de penetrar la membrana de las células tumorales. ¿Y cuál podría ser la posible solución? Pues como muestra este estudio llevado a cabo con un modelo animal –ratones– de carcinoma anaplásico de tiroides, el uso de nanopartículas.
Nuestro trabajo permite que los pacientes con carcinoma anaplásico de tiroides cuenten con algunas opciones
Sareh Parangi
Pero aún hay más. Los autores también cargaron las nanopartículas con un polímero con fluorescencia cercana al infrarrojo, lo que les permitió observar cómo las nanopartículas circulaban durante un largo período de tiempo por el torrente sanguíneo del animal para, finalmente, acumularse en el tumor primario –es decir, en el carcinoma anaplásico original, que no en las posibles metástasis.
Gen ‘silenciado’
Y el uso de este ARNi, ¿es realmente eficaz a la hora de silenciar la expresión del gen ‘BRAF’? Pues sí, y mucho. Y es que el uso de este ARNi en células tumorales cultivadas en una placa de laboratorio no solo conllevó una drástica ralentización de la proliferación tumoral, sino que el número de células con capacidad de migración se redujo en hasta 15 veces. Un resultado que, asimismo, también se observó en los modelos animales, en los que se frenó el crecimiento tumoral y se formaron muchas menos metástasis.
Como concluye Sareh Parangi, co-autora del estudio, « la gran mayoría de pacientes con carcinoma anaplásico de tiroides ya no cuentan con ninguna opción cuando llegan al quirófano . Sin embargo, esta nueva investigación permite que estos pacientes aún tengan algunas opciones. Contar con un enfoque que nos permita una rápida visualización del tumor y, simultáneamente, posibilite su tratamiento dirigido podría ser crítico para un abordaje eficiente no ya solo de esta enfermedad, sino también de otros cánceres letales con un mal pronóstico».
Noticias relacionadas
Esta funcionalidad es sólo para suscriptores
Suscribete
Esta funcionalidad es sólo para registrados
Iniciar sesiónEsta funcionalidad es sólo para suscriptores
Suscribete