DIABETES
Diseñada una terapia génica capaz de normalizar los niveles de glucosa en la diabetes
Un estudio llevado a cabo con ratones muestra cómo reprogramar las células alfa de los islotes pancreáticos en células beta productoras de insulina
M. LÓPEZ
La diabetes tipo 1 es una enfermedad crónica causada por la destrucción por el propio sistema inmunitario del paciente de las células responsables de la producción de insulina –las consabidas células beta de los islotes pancreáticos–. En consecuencia, y dado que esta insulina es la ... hormona responsable de que las células capten la glucosa de la sangre para producir energía, el torrente sanguíneo acaba portando un exceso de glucosa, lo que acaba provocando daños en múltiples órganos del cuerpo. De ahí la importancia de un nuevo estudio dirigido por investigadores de la Facultad de Medicina de la Universidad de Pittsburgh (EE.UU.), en el que se muestra cómo una terapia génica es capaz de mantener unos niveles normales de glucosa en sangre durante mucho tiempo. O así sucede, cuando menos, en modelos animales –ratones.
Noticias relacionadas
Como explica George Gittes, director de esta investigación publicada en la revista « Cell Stem Cell », «básicamente, nuestro estudio es la primera descripción de una sencilla intervención y clínicamente traducible en la diabetes autoinmune que conlleva a una normalización de la glucosa sanguínea . Y lo que es muy importante, sin ningún tipo de inmunosupresión. Dada la notable naturaleza de la reversión de la diabetes, así como la viabilidad de la terapia génica con virus adeno-asociados (AAV) en los pacientes, la posible puesta en marcha de un ensayo clínico en diabetes tipo 1 y tipo 2 en un futuro próximo es ciertamente realista».
Parecidas pero funcionales
El objetivo fundamental del tratamiento de la diabetes tipo 1 es preservar o, en su defecto, restaurar, las células beta pancreáticas productoras de insulina. Sin embargo, el reemplazo de estas células beta está condenado al fracaso dado que las nuevas células serán destruidas, tal y como sucedió con las originales, por la autoinmunidad. Entonces, ¿qué se puede hacer? Pues una posible solución sería reprogramar otras células en células beta funcionales para que, así, puedan producir insulina . Y como estas células reprogramadas no serían realmente células beta, no serían reconocidas por el sistema inmune y, por tanto, no acabarían siendo destruidas. Pero, ¿esto realmente se puede hacer?
Para evaluar esta posibilidad, los autores diseñaron un AAV para que llevaran al páncreas de un modelo animal –ratones– dos proteínas denominadas ‘Pdx1’ y ‘MafA’, implicadas en la maduración, proliferación y funcionalidad de las células beta. Así, el objetivo era tratar de convertir a las células alfa pancreáticas en células beta. Y llegados a este punto, ¿por qué centrarse en las células alfa? Pues porque presentan unas características ‘idóneas’: hay un montón, se parecen mucho a las beta y ya están en el páncreas.
La terapia génica viral crea nuevas células productoras de insulina que son resistentes al ataque autoinmune
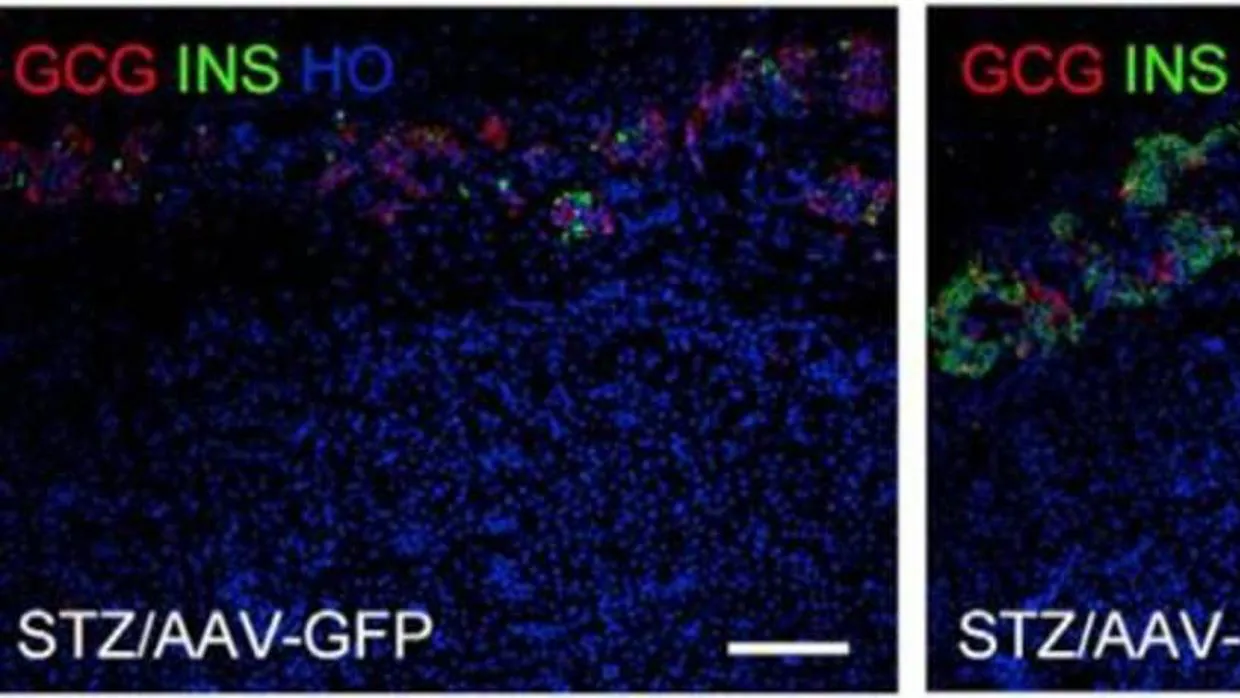
La terapia génica logró restaurar los niveles de glucosa en sangre de los animales a unas cifras normales durante un largo periodo de tiempo –en torno a cuatro meses –. Y para ello, tan ‘solo’ tuvo que generar células funcionales productoras de insulina –en su inmensa mayoría a partir de las células alfa, si bien hubo algunas resultantes de la transformación de otros tipos de células.
Como refiere George Gittes, «la terapia génica viral crea estas nuevas células productoras de insulina que son resistentes al ataque autoinmune. Esta resistencia parece deberse al hecho de que las nuevas células son un poco diferentes a las células normales de la insulina, pero no tan diferentes como para que no funcionen bien ».
Años de normalización
Pero, más allá de los ratones ¿qué pasa con los pacientes? Pues muchos de los aspectos contemplados en la estrategia pueden ser aplicados a los seres humanos. El vector empleado es un AAV similar a los que ya se están utilizando en distintos ensayos clínicos con terapias génicas. Un vector que, además, puede ser inoculado directamente en el páncreas mediante endoscopia, por lo que no es necesaria la cirugía. Y a todo ello se aúna que no se requiere inmunosupresión, por lo que se evitarían algunos efectos secundarios como un mayor riesgo de infecciones.
Sin embargo, la mayor preocupación es que los ratones volvieron con el paso del tiempo a su estado diabético. Es decir, la terapia no ofrece una cura definitiva para la diabetes. Pero como puntualizan los autores, «si bien la protección frente a la diabetes recurrente no fue permanente en los ratones, algunos estudios sugerirían que el proceso se encuentra muy acelerado en estos animales. Así, cuatro meses en los ratones se traduciría en varios años en los humanos ».
Y entonces, ¿cuál sería el siguiente paso? Pues evaluar el procedimiento en animales más grandes. De hecho, los autores ya están probando la nueva terapia génica en primates. Como concluye George Gittes, «si somos capaces de demostrar su eficacia en primates no humanos, entonces nos pondríamos en marcha para lograr la aprobación por la Agencia de Alimentos y Medicamentos de Estados Unidos (FDA) para el uso de esta terapia génica viral en pacientes con diabetes, tanto tipo 1 como tipo 2».
Diseñada una terapia génica capaz de normalizar los niveles de glucosa en la diabetes
Esta funcionalidad es sólo para suscriptores
Suscribete
Esta funcionalidad es sólo para registrados
Iniciar sesiónEsta funcionalidad es sólo para suscriptores
Suscribete